En la Enfermedad Inflamatoria Intestinal 1 (EII) se produce una inflamación del intestino que hace que los neutrófilos acudan a la zona inflamada para actuar. En este entorno inflamado y debido a la disrupción de la barrera intestinal y a su incremento en permeabilidad, los neutrófilos se infiltran en la mucosa intestinal para defender al organismo de la entrada de bacterias procedentes del interior del intestino, y se “suicidan” en un proceso conocido como Netosis, formando NETs , unas estructuras en forma de red, cuya función es destruir al mayor número de bacterias “intrusas” lo más rápidamente posible, liberando todo el contenido intracelular al exterior. Un porcentaje muy elevado del citoplasma de los neutrófilos está formado por calprotectina, que es una proteína muy resistente a la degradación bacteriana y estable a temperatura ambiente durante días. Dicha proteína pasa a la luz del intestino (dado que la barrera intestina ha perdido su integridad) y se elimina del organismo a través de las heces, de ahí su nombre de calprotectina fecal (CF). De este modo, si se miden los niveles de calprotectina en las heces se pude determinar por su concentración, si el paciente está en brote activo o no, e incluso la severidad de la enfermedad.
Autor: Adacyte
Noticias
Calprotectina fecal (CF). ¿Qué es y qué papel juega en la Enfermedad Inflamatoria Intestinal?
7 de marzo, 2024
Patologías

La medida de la CF es muy habitual en el diagnóstico de la EII, para determinar y evaluar el estado y gravedad de la enfermedad. Además, es un biomarcador que permite analizar de una manera no invasiva, los cambios de un paciente a nivel intestinal durante un largo período de tiempo.
¿Cómo se realiza una prueba de calprotectina fecal y cuál es el mejor momento para realizarla?
Dado que la medición de esta proteína se realiza a través de las heces, será necesario tomar una muestra de heces del paciente y analizarla. Las recomendaciones de GETECCU para la recogida de muestras2 son las siguientes:
Se recomienda recoger una pequeña cantidad de heces (aproximadamente 3-5g) y depositarla en un bote de recogida que se dispensa habitualmente en el centro solicitante. Dicho recipiente no requiere ningún tratamiento específico. Se puede tomar la muestra de cualquier parte de la deposición, ya que se ha demostrado que la CF se distribuye de manera homogénea y en cualquier momento del curso de la enfermedad3.
Como precaución y obtención de un resultado fiable, se ha constatado un marcado descenso de los niveles de CF durante la preparación para una colonoscopia4. Por ello, en caso de que el paciente tenga programada una, se debe tener la precaución de recoger la muestra antes de iniciar la limpieza del colon o varios días después de la prueba.
¿Qué significa que la calprotectina fecal esté elevada?
Cuando la CF está elevada en la enfermedad inflamatoria intestinal, significa que existe inflamación en el intestino. Por norma general, niveles altos indican infecciones bacterianas, parasitarias, cáncer colorrectal o determinadas enfermedades que provocan inflamación del intestino, como la colitis ulcerosa5 (CU) y la enfermedad de Crohn6 (EC).
Tanto en la CU como en la EC, su elevación se podría traducir en que la enfermedad está activa y puede estar causando síntomas como dolor abdominal, diarrea o sangrado ya que el sistema inmune está luchando para disminuir dicha inflamación en el intestino.
Ahora que ya entiende qué es la calprotectina fecal, lo más importante es que confíe en su médico, siga el tratamiento pautado y le comunique su sintomatología para que puedan plantear la mejor estrategia en la gestión de su enfermedad y llevar a cabo las pruebas necesarias en cada momento.
- Enfermedad de Crohn y Colitis Ulcerosa: similitudes y diferencias – Adacyte
- Recomendaciones del Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa (GETECCU) sobre la utilidad de la determinación de calprotectina fecal en la enfermedad inflamatoria intestinal | Gastroenterología y Hepatología (elsevier.es)
- Intra-Individual Variability of Faecal Calprotectin: A Prospective Study In Patients With Active Ulcerative Colitis | Journal of Crohn’s and Colitis | Oxford Academic (oup.com)
- Colonoscopia e ileoscopia: pruebas indispensables para diagnosticar EII – Adacyte
- ¿Qué es la Colitis Ulcerosa? – Adacyte
- Enfermedad de Crohn y Colitis Ulcerosa: similitudes y diferencias – Adacyte
Noticias
Colonoscopia e ileoscopia: pruebas indispensables para diagnosticar EII
5 de mayo, 2023
Patient

Diarrea, dolor abdominal, sangre en heces, anemia, fatiga, fiebre, pérdida de peso. Son signos que pueden alertar de algún problema digestivo. En el momento en el que existe la sospecha de que un paciente puede sufrir una enfermedad inflamatoria intestinal (EII), como la colitis ulcerosa o la enfermedad de Crohn, el profesional sanitario necesita de herramientas de diagnóstico fiables que confirmen dichas patologías, descartando otro tipo de dolencias cuya sintomatología es similar.
Además de las pruebas analíticas, tanto la sanguínea como la de heces, y de las pruebas radiológicas, las pruebas endoscópicas son una técnica fundamental e indispensable para el diagnóstico de la EII.
Dentro de estas exploraciones endoscópicas se incluyen la enteroscopia, la ecografía endoanal, la cápsula endoscópica, la endoscopia digestiva alta o gastroscopia y la endoscopia digestiva baja o ileocolonoscopia. Durante las próximas líneas explicaremos en qué consiste esta última técnica que incluye la colonoscopia y la ileoscopia.
La ileocolonoscopia como herramienta de diagnóstico
La ileocolonoscopia es una de las pruebas endoscópicas más habituales que se realizan para diagnosticar la EII. Gracias a ella, los profesionales sanitarios pueden visualizar de forma directa la mucosa intestinal, tanto el colon (colonoscopia) como el final del intestino delgado o íleon terminal (ileoscopia).
Así, es posible saber si el paciente sufre enfermedad de Crohn o colitis ulcerosa porque las características endoscópicas son singulares y diferentes entre sí. Además, ayudan a elegir la opción terapéutica más adecuada y si es necesaria una intervención quirúrgica. La razón es que se visualiza la extensión y severidad de las afectaciones, así como su localización exacta en el colon y el íleon terminal. En el caso de la Enfermedad de Crohn, es habitual que el íleon esté afectado, de ahí la conveniencia de realizar una ileoscopia junto a la colonoscopia en estos casos.
Por otro lado, estas técnicas son herramientas eficaces para descartar afectaciones por fármacos, como los antiinflamatorios, u otro tipo de patologías con síntomas similares, como la colitis infecciosa. Asimismo, en caso necesario es posible tomar biopsias (muestras de tejido) durante la exploración para realizar un estudio anatomopatológico o realizar procedimientos terapéuticos. Es el caso de la polipectomía (extracción de pólipos) o de la dilatación de estenosis (reducción del diámetro interno del intestino).
Monitorización del paciente con EII a largo plazo
Realizar un seguimiento de la evolución de la enfermedad inflamatoria a largo plazo es fundamental para anticiparse a los brotes, valorar la eficacia del tratamiento que está siguiendo el paciente y modificarlo si fuera necesario. Y en este caso es de gran utilidad la ileocolonoscopia porque permite visualizar la extensión y la evolución de la afectación del colon y el final del intestino delgado o íleon terminal.
Cuando el paciente presenta una EII de larga evolución tiene más probabilidades de desarrollar cáncer colorrectal que la población general. Un riesgo que es mayor o menor según la duración y la extensión de la enfermedad. Por eso, la vigilancia endoscópica mediante la ileocolonoscopia puede ser una herramienta eficaz para detectar lesiones premalignas y actuar lo antes posible, reduciendo así la mortalidad asociada al cáncer colorrectal. Otra de las situaciones en las que es de gran utilidad la realización de una ileonoscopia es tras una cirugía. De hecho, es considerado el ‘patrón oro’ porque permite establecer la aparición de la recurrencia morfológica y su gravedad, relacionada directamente con la evolución clínica a largo plazo1.
¿Cómo debe prepararse el paciente para la prueba?
Al igual que cualquier procedimiento endoscópico, tanto la colonoscopia como la ileoscopia precisan que el paciente realice una preparación previa a la prueba. Dichos preparativos pasan por llevar una dieta especial y, en ocasiones, la supresión de algunos medicamentos que esté tomando. En este último caso, el profesional médico le informará cómo debe proceder con dichos fármacos para evitar complicaciones y que puedan dificultar la exploración.
En cuanto a la dieta previa2 que el paciente debe seguir, dos días antes de la prueba debe iniciar una dieta baja en residuos. Esto quiere decir que se prohíben quesos grasos, productos lácteos enteros, pescados azules, carnes grasas, embutidos, productos integrales, frutas, verduras, legumbres, chocolate, pasteles y frutos secos.
Por otro lado, los alimentos que sí puede tomar durante la dieta especial son: leche y yogur natural desnatados, quesos frescos, quesos duros y un poco de mantequilla; pan blanco o tostado y galletas no integrales; caldos sin verduras; arroz y pastas no integrales; patatas en puré o cocidas, sin la piel; carnes y pescados blancos a la plancha o cocidos; membrillo, melocotón en almíbar, manzana o pera cocida o asada, sin piel; té, café e infusiones ligeras.
El día anterior a la colonoscopia o la ileoscopia, se empezará con la limpieza intestinal con preparados indicados por el profesional médico. Éstas pueden ser soluciones de polietilenglicol, sales de magnesio, soluciones de fosfato sódico o enemas. Pero 3 o 4 horas antes de iniciar la limpieza intestinal, el paciente debe dejar de tomar alimentos sólidos.
A partir de ese momento solo puede tomar líquidos claros, es decir, agua, infusiones, caldos filtrados, café o té, zumos de fruta colados y bebidas refrescantes claras. El día de la prueba, el paciente debe dejar de tomar líquidos claros unas 3-4 horas antes de realizarse la colonoscopia o la ileoscopia.
Durante y después de la ileocolonoscopia
La prueba se realiza en la Unidad de Endoscopias del Servicio de Digestivo. La llevan a cabo médicos especialistas en Digestivo con formación en endoscopia diagnóstica y terapéutica de la propia Unidad de EII o, en su defecto, con formación EII.
También participa personal de enfermería especializado en endoscopia y auxiliares de enfermería. Su función durante la ileocolonoscopia es cuidar y atender al paciente, ayudar al endoscopista a la realizar la prueba y administrar la medicación necesaria.
En cuanto a la duración de la exploración, puede oscilar entre los 20 y 60 minutos. Este tiempo depende de la cantidad de intestino a explorar y de si es necesario realizar algún procedimiento terapéutico durante la exploración. Además, con el objetivo de evitar molestias al paciente y posibilitar que la prueba se lleve a cabo sin dolor, se suele administrar sedación y analgesia intravenosa.
Finalizada la prueba, el paciente es llevado a otra sala donde se despertará con una sensación de hinchazón abdominal y molestias similares a un cólico intestinal. Esto se debe al aire insuflado dentro del intestino durante la exploración. Son molestias que irán desapareciendo a las pocas horas.
Noticias
¿Qué es la Colitis Ulcerosa?
21 de marzo, 2023
Patologías

La Colitis Ulcerosa1 es un tipo de Enfermedad Inflamatoria Intestinal (EII) que afecta a la mucosa del colon (intestino grueso). La mucosa es la encargada de ejercer de barrera ante sustancias dañinas. También ayuda en la absorción y transporte de nutrientes, agua y minerales; y lubrica el interior del intestino para facilitar la defecación. Su inflamación se produce debido a que el sistema inmune genera una respuesta inflamatoria exagerada frente al propio organismo. El origen de este fallo en las respuestas del sistema inmune intestinal no es del todo conocido.
Cuando la mucosa se inflama, se desarrollan pequeñas heridas (úlceras) en el revestimiento interior del colon. Esta inflamación crónica comienza en el recto y se extiende por otros tramos del colon (ascendente, transversal y descendente). Es decir, esta afectación es de extensión variable.
Los síntomas de la colitis ulcerosa más comunes son las heces líquidas con moco y/o sangre, el dolor intestinal, el esfuerzo al defecar, la fiebre, la pérdida de peso y el cansancio. Además, podrán estar afectados otros órganos como la piel, los ojos, los huesos, etc. La mayoría de las personas que sufren CU presentan síntomas leves a moderados. Existirán periodos de actividad en los que los síntomas estén presentes (llamados brotes2). Sin embargo, también hay periodos de normalidad en los que la enfermedad parece desaparecer (llamados fases de remisión). Algunas personas pueden tener largos períodos de remisión.
Factores de riesgo
Al igual que la Enfermedad de Crohn (EC), la CU es un trastorno propio de las sociedades más desarrolladas. De hecho, su frecuencia en los países desarrollados ha ido en aumento desde mediados del siglo XX. Esta enfermedad afecta aproximadamente en la misma proporción a mujeres que a hombres. Los factores de riesgo pueden ser:
- Edad. Aunque puede aparecer a cualquier edad, generalmente comienza antes de los 30 años. Sin embargo, también hay casos en los que la enfermedad se ha diagnosticado después de los 60 años.
- Raza u origen étnico. Aunque las personas caucásicas tienen un mayor riesgo de padecer la enfermedad, cualquier otra etnia puede presentarla. Curiosamente, la ascendencia judía askenazí, presenta un riesgo mayor.
- Antecedentes familiares. Es frecuente encontrar casos de CU entre miembros de una misma familia. Entre un 8 y 14% de pacientes con CU tienen un antecedente familiar de EII. El riesgo aumenta cuando tienes un pariente cercano (padre, hermanos o hijos) con esta enfermedad.
Causas de Colitis Ulcerosa y otras cuestiones desconocidas para la ciencia
Aunque la ciencia ha realizado grandes esfuerzos por conocer la causa o causas de la aparición de la colitis ulcerosa3, estasson todavía desconocidas. La ciencia sigue preguntándose cuál es la causa concreta de la respuesta inflamatoria inadecuada o exagerada del sistema inmune. Según Geteccu4, as investigaciones actuales apuntan a que la enfermedad puede surgir como resultado de una compleja interacción entre varios factores5.
Uno de estos factores es la predisposición genética (susceptibilidad) de una persona a padecer la enfermedad. Pero también parece ser clave que aparezca CU tras la exposición a factores ambientales (por ejemplo, el tabaco), la microflora comensal intestinal y la posible participación de agentes infecciosos. Se cree que dichas alteraciones genéticas afectan a la habilidad del sistema inmune para tolerar las bacterias comensales y afectan también la intensidad de la respuesta inflamatoria frente a dichas bacterias. Sin embargo, el origen genético todavía no está del todo claro.
Junto a esta cuestión, existen otras preguntas sobre patogénesis de la CU que todavía plantean un reto para la ciencia. ¿Por qué la inflamación está restringida a la capa mucosa? ¿Son las células epiteliales del colon el objetivo específico de una respuesta inmunológica? ¿Cómo afecta la microbiota intestinal a la respuesta inflamatoria?
- https://educainflamatoria.com/category/colitis-ulcerosa/
- ¿Cómo actuar en caso de sufrir un brote de colitis ulcerosa? – Adacyte
- Causas de la colitis ulcerosa: ¿Qué factores desencadenan la enfermedad? – Adacyte
- https://geteccu.org/
- https://educainflamatoria.com/colitis-ulcerosa/causas-y-factores-influencia/
Noticias
¿Cuáles son las manifestaciones extraintestinales oftalmológicas más prevalentes relacionadas con EII?
16 de marzo, 2023
Patologías
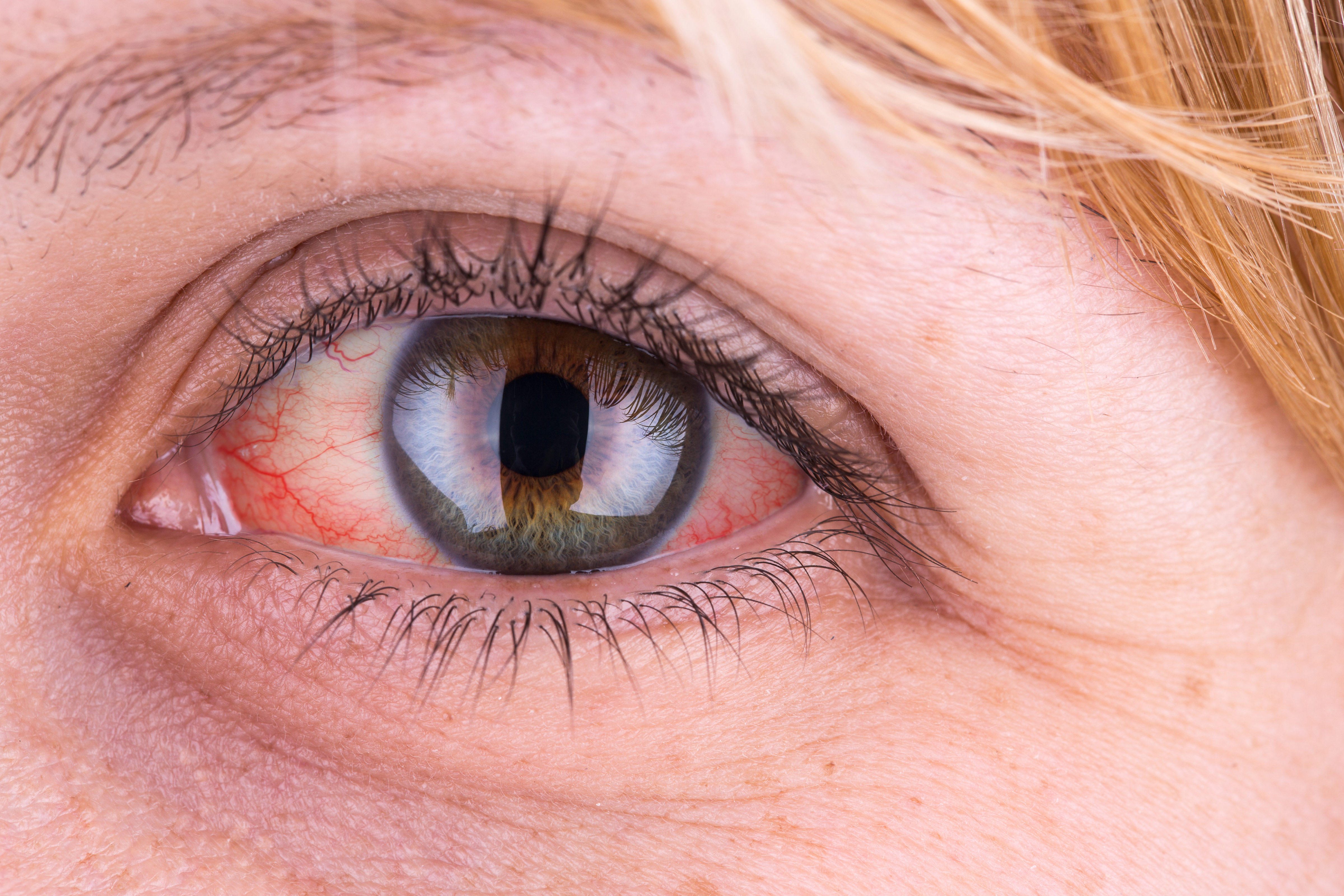
La enfermedad inflamatoria intestinal (EII) se considera una enfermedad inflamatoria sistémica. Es decir, que además de la afectación del intestino también se pueden desarrollar patologías en otros órganos y sistemas como el ocular. Son las conocidas como manifestaciones extraintestinales (MEI), enfermedades que no tienen por qué estar ligadas íntimamente a la actividad inflamatoria del intestino a pesar de producirse de forma simultánea. De hecho, sus mecanismos desencadenantes no se conocen con exactitud, aunque se cree que la causa puede estar relacionada con la interacción de factores genéticos, ambientales y cambios en la microbiota intestinal.
Las manifestaciones extraintestinales oftalmológicas son poco frecuentes en pacientes con EII afectando tan solo al 10%1. La consecuencia de esta baja prevalencia es que tanto los profesionales médicos como los propios pacientes pasan por alto la posibilidad de que síntomas como dolor o enrojecimiento ocular sean sintomatología relacionada con colitis ulcerosa2 o enfermedad de Crohn. Un error que puede tener consecuencias graves para los enfermos y que son evitables con un abordaje multidisciplinar en el que se incluya un examen oftalmológico completo.
Las alteraciones oculares más comunes en pacientes con EII son la escleritis, la epiescleritis y la uveítis. En los dos primeros casos, la estructura ocular afectada es la esclera, conocida como parte blanca del ojo; y en la uveítis la afectación se encuentra en la úvea, la capa situada bajo la esclera. Cabe destacar que la aparición de las tres afecciones suele coincidir con otras manifestaciones cutáneas y articulares, lo que puede dar una pista para la detección precoz de patologías oculares.
Síntomas y tratamiento de la epiescleritis y la escleritis
La epiescleritis y la escleritis son manifestaciones extraintestinales oftalmológicas que afectan a la parte blanca del ojo, aunque cada una de ellas lo hace en un grado diferente.
La epiescleritis se produce cuando la delgada capa de tejido que cubre la parte blanca del ojo (epiesclera) se inflama y se irrita. Una inflamación que suele coincidir con un brote de la enfermedad. Su sintomatología destaca por la sensación de ardor en el ojo que con la palpación no empeora, el enrojecimiento, el lagrimeo y el dolor o molestia leve.
El tratamiento de la epiescleritis depende de la gravedad de los síntomas. Normalmente la afección se cura con el propio tratamiento de la EII aunque en ocasiones se combina con colirios antiinflamatorios no esteroideos para aliviar las molestias.
Si la epiescleritis no se trata a tiempo y de forma correcta es probable que derive en escleritis, un problema ocular más grave que puede ocasionar pérdida de visión. Los síntomas de la escleritis son dolor grave del ojo que empeora con la palpación y se irradia hacia la frente, la mejilla o los senos paranasales; y mayor enrojecimiento del ojo que en la epiescleritis.
Para tratar y controlar la escleritis, además del propio tratamiento de la colitis ulcerosa y de la Enfermedad de Crohn, se prescriben corticoides sistémicos, antiinflamatorios no esteroideos (AINE) o inmunosupresores como el metotrexato.
Cómo detectar la uveítis
La uveítis es otra de las manifestaciones extraintestinales oftalmológicas más prevalentes en pacientes con EII. Suele aparecer tanto en periodos de remisión como durante los brotes o incluso antes del diagnóstico de la propia enfermedad inflamatoria. Se caracteriza por la inflamación de la capa situada bajo la parte blanca del ojo, la úvea, en la que se encuentran gran cantidad de vasos sanguíneos.
Cuando la inflamación se produce en la parte frontal del ojo se conoce como uveítis anterior. Es la más frecuente y los síntomas son enrojecimiento de los ojos, sensibilidad a la luz (fotofobia), dolor ocular, lagrimeo y visión borrosa. Si a esta sintomatología se une la disminución de la visión y/o la aparición de moscas volantes es posible que el paciente sufra uveítis posterior.
Si se experimenta alguno de los síntomas descritos anteriormente se debe acudir al médico cuanto antes porque las consecuencias pueden ser graves, llegando incluso a sufrir la pérdida permanente de la visión. La sintomatología puede presentarse de forma repentina y empeorar en poco tiempo o bien puede iniciarse de manera gradual. De ahí que suponga una urgencia oftalmológica y la necesidad de contar con un diagnóstico precoz para evitar complicaciones.
El tratamiento de la uveítis pasa por la aplicación de colirios ciclopléjicos que sirven para aliviar el dolor y evitar adherencias oculares posteriores (sinequias). Junto a ellos se suelen utilizar corticoides tópicos, oculares, perioculares o sistémicos e incluso inmunosupresores para los casos más graves.
Noticias
Planificar un embarazo en mujeres con EII
6 de febrero, 2023
Patient

Cuando se decide tener hijos se dibujan en el horizonte dudas respecto a la planificación, el embarazo en sí, el parto o la lactancia materna. Una nueva fase en la vida que, si bien llega con mucha ilusión y esperanza, no está exenta de miedos e incertidumbre. Quizá uno de los principales temores de los futuros padres y madres sea la posibilidad de que el bebé nazca con algún tipo de patología que pueda afectar a su calidad de vida.
De ahí la importancia de planificar un embarazo, sobre todo cuando hablamos de pacientes con enfermedad inflamatoria intestinal (EII) como la colitis ulcerosa o la enfermedad de Crohn. En estos casos, aunque la mayor parte de los embarazos en pacientes con EII son exitosos y sin complicaciones, es indispensable realizar una consulta previa a la concepción con los profesionales sanitarios para que valoren el estado en el que se encuentra la paciente, cuándo es aconsejable que se quede embarazada o cuáles son los factores de riesgo, además de explicar qué complejos vitamínicos necesita durante la gestación.
En este artículo vamos a explicar con detalle los aspectos a tener en cuenta por parte de los pacientes con EII, principalmente las mujeres, cuando desean tener hijos.
Primer paso: la planificación del embarazo
Las parejas en las que al menos uno de los dos progenitores tenga EII deben planificar el embarazo para establecer ciertos cuidados y controles, tanto de la madre como del feto. Algunos de esos chequeos comprueban que la paciente no tenga déficits de vitamina B12, hierro y ácido fólico, entre otros macro y micronutrientes. Además de este punto tan importante, es necesario detectar si la paciente sufre displasia (crecimiento de células anormales en un tejido u órgano) o carcinoma cérvico-uterino y de colon porque eso afectará directamente a su embarazo.
Por otro lado, cabe destacar, quizá por encima de otros factores, que el mayor riesgo para la madre y el feto es que la EII se encuentre activa. Por eso la paciente nunca debe abandonar el tratamiento de motu propio. Ni antes, ni durante el embarazo porque podría sufrir una recidiva. Y es que, la mayoría de los embarazos complicados (parto prematuro, bajo peso del recién nacido) están relacionados con el propio proceso inflamatorio. De ahí que sea un aspecto fundamental. Para lograr que el embarazo se desarrolle con la mayor normalidad posible y evitar riesgos, la responsabilidad del cuidado y control de las embarazadas recae en un equipo multidisciplinar formado por gastroenterólogos y cirujanos especializados en EII, así como de obstetras expertos en embarazos de alto riesgo y pediatras en recién nacidos con progenitores con enfermedades inflamatorias intestinales.
La fertilidad: EII activa vs EII inactiva
La mayor parte de los estudios que se han realizado sobre fertilidad en hombres y mujeres con EII demuestran que la fertilidad no se ve afectada cuando la enfermedad está inactiva. De hecho, son igual de fértiles que la población general. Es más, un embarazo sin complicaciones es posible siempre y cuando la enfermedad no esté activa.
Sin embargo, es habitual que el miedo a los efectos adversos sobre el feto derivados de los fármacos, a tener un brote durante la gestación o a no poder compatibilizar la enfermedad con los hijos, lleve a los pacientes a tomar la decisión de no tener descendencia. De ahí que más que infertilidad, que el número de embarazos en pacientes con colitis ulcerosa o enfermedad de Crohn sea inferior a la población general se deba principalmente a una decisión meditada y tomada en el seno de cada pareja. También es un obstáculo, y otra razón por la que los pacientes con EII inactiva deciden voluntariamente no ser padres, la idea de que el bebé pueda desarrollar su enfermedad. En este sentido, si tan solo un progenitor tiene EII, la posibilidad de que el niño o la niña desarrolle la enfermedad es menor al 5,2%. Porcentaje que aumenta hasta un 33% si ambos padres sufren alguna de enfermedad inflamatoria intestinal1.
En el lado opuesto se encuentran los pacientes con EII activa cuya fertilidad sí puede verse afectada. En ocasiones el propio brote o encontrarse en una situación de desnutrición pueden ser los factores que disminuyan la fertilidad, aunque no son los únicos. Otros mecanismos que pueden influir en ella son la extensión de la inflamación hacia las trompas de Falopio y ovarios en la enfermedad de Crohn o cuando el coito es doloroso (dispareunia) debido a que la enfermedad perianal está activa o se han formado adherencias en la pelvis tras cirugías como la proctocolectomía con reservorio íleo-anal. A pesar de este escenario oscuro existen estudios que ofrecen esperanza a las pacientes sometidas a proctocolectomía con reservorio íleo-anal que tienen problemas para concebir. En estos casos, las técnicas de fecundación in vitro son una posibilidad que pueden considerar porque las tasas de embarazo son similares a las de pacientes con colitis ulcerosa, con o sin reservorio íleo-anal2.
Las pacientes no deben abandonar, bajo ningún concepto, su tratamiento cuando están embarazadas sin antes consultarlo con su profesional médico. ¿Por qué? Porque dejar o discontinuar la medicación por decisión propia es peor y más perjudicial que los posibles efectos adversos del tratamiento.
A pesar de que actualmente la mayoría de los fármacos se consideran seguros durante el embarazo y la lactancia, no son compatibles con el embarazo: Metotrexato, Tofacitinib, Talidomida, 6-Tioguanina (embarazo) y Ciclosporina (lactancia). En el caso de los hombres, el tratamiento con sulfasalazina puede afectar, de forma reversible, al número y movimiento de los espermatozoides.
Para evitar llegar a esta situación en la que el/la paciente esté tomando fármacos contraindicados para la gestación o pueda abandonar el tratamiento por su cuenta, el sanitario debe saber, tal y como hemos explicado anteriormente, la intención de tener hijos de los pacientes, porque solo así podrá modificar el tratamiento y sustituirlo por otros medicamentos o técnicas como la aféresis leucocitaria que si sean compatibles con el embarazo. Este último procedimiento, el de la granulocitoaféresis, es un tratamiento no farmacológico que consiste en eliminar los tipos celulares o mediadores inflamatorios del torrente sanguíneo a través del paso de la sangre por una columna que esta rellena de esferas de acetato de celulosa las que /donde diversas subpoblaciones leucocitarias inflamatorias quedan adsorbidas/retenidas. Este proceso es un tratamiento no farmacológico que ofrece una alternativa eficaz y segura a los pacientes que no responden a otros tratamientos o, como en el caso de las mujeres embarazadas, no pueden tomar ciertos fármacos por los efectos secundarios que provocan.
- FERTILIDAD Y EMBARAZO EN PACIENTES CON ENFERMEDADES INFLAMATORIAS INTESTINALES | Revista Médica Clínica Las Condes (elsevier.es)
- In Vitro Fertilization Is Successful in Women With Ulcerative Colitis and Ileal Pouch Anal Anastomosis – PubMed (nih.gov)
- FERTILIDAD Y EMBARAZO EN PACIENTES CON ENFERMEDADES INFLAMATORIAS INTESTINALES | Revista Médica Clínica Las Condes (elsevier.es)
Noticias
Granulocitoaféresis en pacientes con colitis ulcerosa
10 de enero, 2023
Adacolumn

El camino que recorren los pacientes con enfermedad inflamatoria intestinal (EII) y sus familiares después de ser diagnosticados con colitis ulcerosa o enfermedad de Crohn es arduo. Asumir la noticia que han recibido, acudir a todas las consultas de especialistas, realizarse las pruebas pertinentes para conocer el alcance de la enfermedad o el tiempo que se tarda en ajustar y establecer el tratamiento correcto, son solo algunos de los obstáculos y retos que deben superar. Y, precisamente, acertar y recibir el tratamiento adecuado es uno de los puntos más complejos al que se tiene que enfrentar el paciente.
Centrándonos en el caso de la colitis ulcerosa, patología que produce la inflamación del recto y el colon, el paciente sufre recidivas con brotes de actividad más o menos intensos, y más o menos duraderos. Los fármacos que actualmente forman parte del arsenal terapéutico del profesional sanitario para tratar a los pacientes, buscan inducir la remisión de esos brotes y mantener inactiva la EII para mejorar la calidad de vida del enfermo. Y, por supuesto, siempre con la mayor eficacia y seguridad posible.
Teniendo en cuenta que algunos pacientes no responden a los tratamientos convencionales o incluso que debido a su perfil no pueden hacer uso de ellos, los profesionales sanitarios han visto en la granulocitoaféresis (GMA) un aliado terapéutico con garantías de éxito en pacientes con colitis ulcerosa. Y esto se debe a que la técnica reduce la cantidad de células inflamatorias existente en el torrente sanguíneo sin necesidad de introducir un fármaco en el paciente.
¿En qué consiste la granulocitoaféresis?
Como hemos escrito en líneas anteriores, la GMA es un tratamiento no farmacológico cuyo fundamento es pasar la sangre del paciente a través de un dispositivo extracorpóreo con la finalidad de eliminar de ella aquellos componentes patógenos que condicionan o perpetúan la enfermedad y de esto modo contribuir a su tratamiento.
Uno de los sistemas de granulocitoaféresis comercializados en Europa es un sistema que se compone de una columna o filtro con esferas de acetato de celulosa que permite la adsorción selectiva de un 65% de granulocitos, un 55% de monocitos/macrófagos y un 2% de linfocitos, eliminándolos así del torrente sanguíneo. El procedimiento consiste en extraer la sangre de la vena cubital del paciente, que circula por el circuito y la columna de adsorción para ser depurada, y se reinfunde a través de la vena cubital contralateral (fig.1, incluimos imagen del proceso).
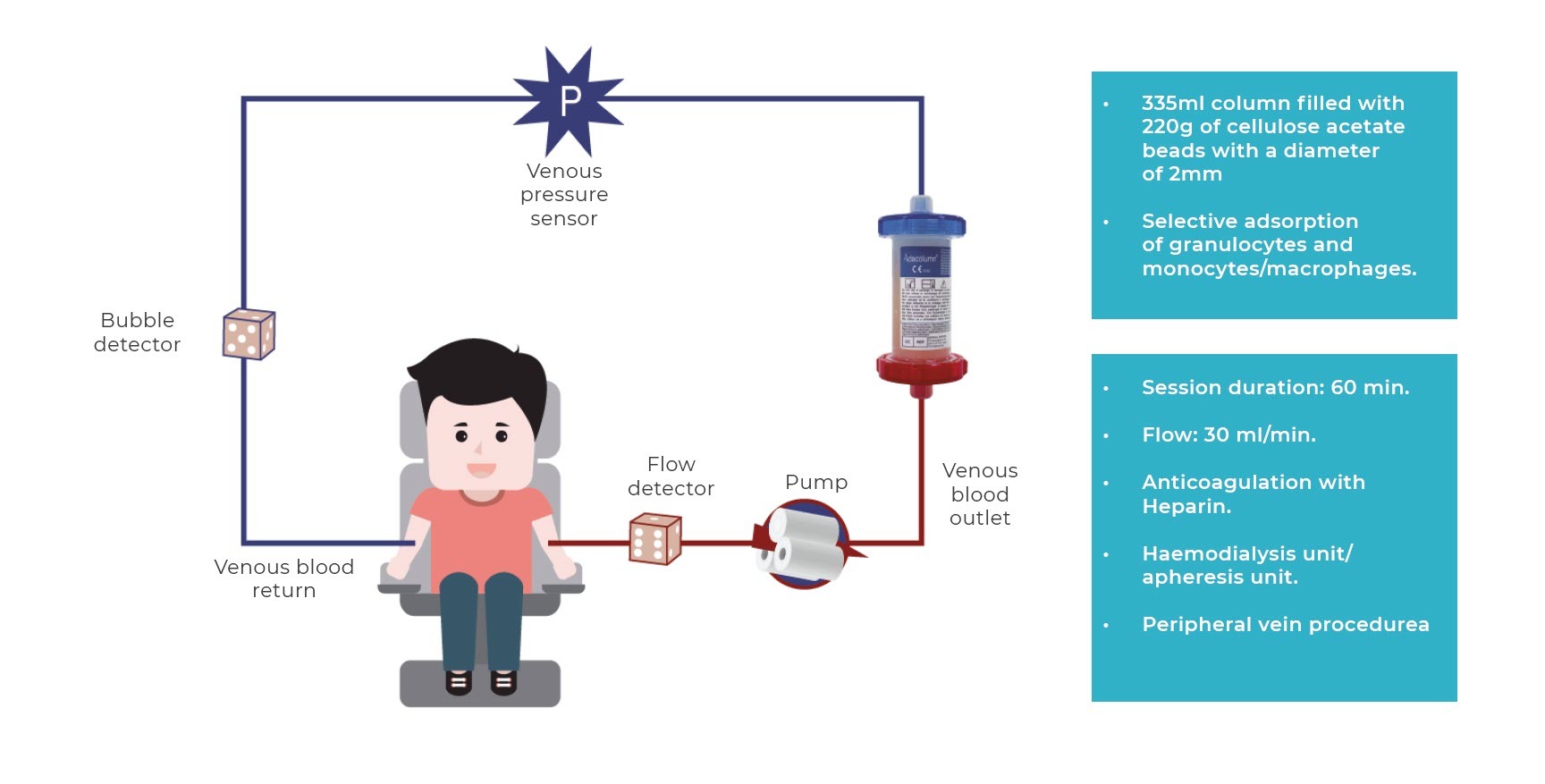
El procedimiento se realiza en unidades de hemodiálisis o bancos de sangre, aunque tras una formación adecuada se puede realizar en unidades de tratamiento en régimen de hospital de día. La pauta de aplicación de la técnica (frecuencia y número de sesiones), va desde 5 sesiones a 10 (1 o 2 por semana) de 60º más minutos de duración, aunque la práctica clínica real en la mayoría de hospitales consiste en una inducción de 10 sesiones (las primeras 3 semanas 2 sesiones/semana para acelerar la respuesta y luego 1 sesión semanal hasta completar las 10) y de mayor duración (normalmente de 90 minutos), ya que se ha observado que este régimen es seguro y bien tolerado, obteniéndose mejores resultados clínicos.
Sin embargo, la única limitación práctica para su realización es la mala accesibilidad para canalizar vías periféricas, lo que podría obligar a colocar una vía central.
En la actualidad aún no se conoce de forma exacta el mecanismo de acción de la GMA. Se sabe, no obstante, que los granulocitos y los monocitos/macrófagos se encuentran elevados y activados en sangre periférica en muchas de las enfermedades autoinmunes, que su número se correlaciona con la actividad y con la gravedad de la enfermedad y que desempeñan un papel clave en la inmunopatogénesis en tanto que producen elevadas cantidades de citocinas proinflamatorias responsables de la lesión tisular.
Se cree que el mecanismo principal de adsorción de la GMA está relacionado con la activación de la cascada del sistema del complemento y con la inducción de la adhesión de los granulocitos a la columna.
Los leucocitos que expresan el receptor Fc gamma (FcγR) y receptores del complemento (Mac-1, CD11b/CD18) se adhieren a las cuentas de acetato de celulosa a través de la activación del complemento. De este modo, la disminución del reservorio de granulocitos activados en la circulación sistémica se compensa con la movilización, desde la médula ósea al torrente circulatorio, de granulocitos jóvenes, no activados (CD10–), sin capacidad de migrar al foco inflamatorio.
Asimismo, se produce un cambio funcional en los monocitos activados, que expresan marcadores CD14+CD16+, lo que en su conjunto conlleva una reducción de la producción de citocinas proinflamatorias y un incremento de mediadores antiinflamatorios circulantes; en definitiva, un fenómeno de inmunomodulación y consiguientemente una reducción del infiltrado inflamatorio y del daño tisular.
La consecuencia directa de la eliminación de leucocitos del sistema circulatorio es la movilización por parte de la médula ósea de leucocitos jóvenes inactivados que no pueden migrar al foco inflamatorio. Adicionalmente el paso de la sangre a través de la columna, además de disminuir el número total de células inflamatorias en la sangre también produce cambios en la superficie de las que retornan al organismo induciendo una serie de cambios a nivel inmunológico que promueven la activación de mecanismos antinflamatorios que estaban inhibidos, poniendo en marcha la resolución de la inflamación. Con ello, además de producir inmunomodulación (cambio que se produce en el sistema inmunitario), se reduce la inflamación y el daño tisular (de las células) en la mucosa intestinal.
¿En qué pacientes está indicado el uso de la GMA?
Actualmente, existe un arsenal terapéutico muy amplio para el tratamiento de la EII aunque en una proporción de pacientes estas medicaciones son ineficaces o presentan efectos adversos2. Por lo tanto, se necesitan otras opciones terapéuticas para controlar la progresión de la enfermedad y evitar intervenciones quirúrgicas.
Otra alternativa para el tratamiento de esta patología en determinados escenarios es la GMA. Esta técnica puede aplicarse en diferentes situaciones, incluyendo aquellos pacientes que no responden adecuadamente a los tratamientos farmacológicos convencionales, o presentan un curso corticodependiente, prevención de recidiva y en los que se plantea iniciar tratamiento inmunosupresor o biológico3,4.
A pesar de buscar el mejor tratamiento para cada caso, existe un alto porcentaje de pacientes con colitis ulcerosa que no responden a los tratamientos convencionales, ya sea a aquellos basados en corticoides o en inmunomoduladores (IMM) tiopurínicos (Ardizzone et al, 2006) o a la terapia anti-TNF. Hasta hace unos años, cuando un profesional sanitario se encontraba en esta situación en la que los medicamentos no lograban mejorar la situación de los pacientes, la opción más utilizada para tratarlo y mejorar su calidad de vida era la cirugía.
Pero en las últimas décadas han surgido otras alternativas de tratamiento en pacientes con colitis ulcerosa, como la GMA, que son más seguras y que pueden aplicarse a los siguientes pacientes1:
- Pacientes adultos con colitis ulcerosa corticodependientes tras el fracaso, intolerancia o riesgo elevado de los tratamientos inmunomoduladores y/o biológicos2.
- Pacientes de edad avanzada con comorbilidades.
- Pacientes embarazadas.
- Pacientes pediátricos con colitis ulcerosa.
Las contraindicaciones son:
- Cifra de granulocitos inferior a 2000/Ml
Las advertencias son:
- Alergia a la heparina y trombopenia dependiente de heparina
- Anemia significativa (Hb < 8 g/dL)
- Coagulopatía grave
- Infección activa
- Enfermedad cardiaca o renal grave
Precauciones:
Precaución en situaciones de hipercoagulabilidad (fibrinógeno > 700 mg/mL) o deshidratación (diarrea o procesos febriles recientes). Deben corregirse previamente estos factores.
GMA, significado de eficacia y seguridad en el tratamiento de la CU
Si hay dos características que definen la GMA son su seguridad y su eficacia. Según recoge el Proyecto Prodiggest3 esta opción terapéutica ha sido objeto de estudios y metaanálisis que permiten describirla como una alternativa eficaz y segura para los pacientes.
Por un lado, se describe la GMA como muy segura para los pacientes con colitis ulcerosa porque los efectos adversos de los tratamientos convencionales desaparecen. En este caso los efectos secundarios son en su mayoría leves y transitorios, por lo que el paciente puede continuar con el tratamiento. Entre ellos destacan la cefalea, los escalofríos, la febrícula, los mareos, la fatiga, las mialgias, las palpitaciones, la hipotensión o el enrojecimiento. En muchos casos los efectos adversos están más relacionados con la técnica de aféresis que con el propio tratamiento de GMA (problemas con las vías…etc), de ahí la importancia de que sea realizada por profesionales expertos.
Por otro lado, además de su eficacia en pacientes pediátricos, embarazadas, ancianos o pacientes corticodependientes y corticorrefractarios, existen otros escenarios donde la GMA es eficaz. Por ejemplo, se ha comprobado que puede ser un tratamiento de primera línea con una tasa de inducción a la remisión del 70% en colitis ulcerosa distal con actividad leve moderada (Yamamoto et al 2004) y hasta el 80% en pacientes con enfermedad poco evolucionada, naïve a esteroides (Takemoto et al 2007), tal y como se recoge en el Proyecto Prodiggest.
Además, es una opción que puede prevenir la recidiva en determinados casos de pacientes con un alto riesgo de sufrir brotes de forma recurrente y difíciles de controlar. En este sentido, se puede establecer una duración media de la remisión clínica en pacientes con colitis ulcerosa obtenida con la GMA de 10 meses (Ljung et al 2007) pudiendo llegar a ser incluso muy superior al año cuanto más inicial sea la enfermedad o menos tratamientos se hayan administrado al paciente con anterioridad (corticoides, tiopurinas, biológicos…etc) a la GMA.
- https://www.aegastro.es/publicaciones/publicaciones-aeg/protocolos-asistenciasles-prodiggest/uso-racional-de-la-granulocitomonoaferesis-en-la-enfermedad-inflamatoria-intestinalhttps://www.aegastro.es/publicaciones/publicaciones-aeg/protocolos-asistenciasles-prodiggest/uso-racional-de-la-granulocitomonoaferesis-en-la-enfermedad-inflamatoria-intestinal
- Tratamiento de la colitis ulcerosa en pacientes dependientes de corticoides y fracaso previo a biológicos: Adacolumn® – Adacyte
- https://www.aegastro.es/publicaciones/publicaciones-aeg/protocolos-asistenciasles-prodiggest/uso-racional-de-la-granulocitomonoaferesis-en-la-enfermedad-inflamatoria-intestinal
- Dignass A, Lindsay JO, Sturm A, Windsor A, Colombel JF, AllezM, et al. Second European evidence-based consensus on thediagnosis and management of ulcerative colitis part 2: Currentmanagement. J Crohns Colitis. 2012;6:991—1030.
- Dignass A, Akbar A, Hart A, et al. Safety and efficacy of granulocyte/monocyte apheresis in steroid-dependent active ulcerative colitis with insufficient response or intolerance to immunosuppressants and/or biologics [the ART trial]: 12-week interim results. J Crohns Colitis. 2016;10:812–820.
- Dittrich K, Richter M, Rascher W, et al. Leukocytapheresis in a girl with severe ulcerative colitis refractory to corticosteroids, infliximab, and cyclosporine A. Inflamm Bowel Dis. 2008;14:1466–1467.
Noticias
La enfermedad inflamatoria intestinal en pacientes de edad avanzada
13 de diciembre, 2022
Patient

Cuidar la alimentación y mantenerse físicamente activo son las dos claves para llevar un estilo de vida saludable. Este hecho que, si bien, es importante a cualquier edad, lo es más aún si queremos llegar a la vejez en buenas condiciones de salud. Y es que, en esta etapa, sobre todo a partir de los 60 años, es posible que debuten patologías como la enfermedad inflamatoria intestinal (EII). De los pacientes en edad avanzada que son diagnosticados por primera vez de colitis ulcerosa1 o de enfermedad de Crohn el 65% tiene entre 60 y 69 años; el 25% entre 70 y 79 años; y el 10% supera los 80 años.2
Las enfermedades inflamatorias intestinales suelen ir acompañadas de otro tipo de patologías secundarias conocidas como manifestaciones extraintestinales (MEI) que afectan a la piel, los ojos o las articulaciones, aunque en pacientes ancianos son menos frecuentes. También lo son las intervenciones quirúrgicas, la recurrencia postquirúrgica y la aparición de las formas más agresivas o graves de la EII.
Malnutrición, anemia y osteoporosis en pacientes mayores con EII
En las personas mayores, sobre todo en aquellas que sufren EII, llevar una alimentación3 variada, completa y equilibrada es fundamental, pero no siempre es factible. Pueden surgir problemas en el proceso de masticación y deglución debido a la pérdida de dientes y a la disminución de la salivación o puede empeorar el proceso digestivo motivado por una reducción de la cantidad y la calidad de las secreciones digestivas que, acompañados por una atrofia la mucosa intestinal, da lugar a una peor absorción y a un menor aprovechamiento de algunos nutrientes, principalmente de proteínas, vitaminas y minerales.
Surge así un problema de malnutrición debido a un empobrecimiento de la dieta que provoca anemia4. Aunque no es el único motivo. Los pacientes de edad avanzada con EII también pueden sufrir anemia y malnutrición por pérdidas de sangre a través del tracto gastrointestinal. De ahí la necesidad de que los pacientes mayores con colitis ulcerosa y Enfermedad de Crohn aseguren el aporte del hierro a través de la ingesta diaria de alimentos ricos en este mineral, destacando el pescado, la carne y los huevos.
La malnutrición en pacientes mayores con EII también es una de las causas de la aparición de osteoporosis. Y es que, la falta de calcio, fósforo, magnesio, vitamina D, entre otros elementos necesarios en la formación de los huesos, influyen en la pérdida de la densidad mineral ósea y el debilitamiento o fragilidad ósea, aumentando así el riesgo de sufrir fracturas.
Para prevenir la osteoporosis en pacientes mayores de 60 años se recomienda dejar de fumar, tener un aporte correcto de calcio y vitamina D y realizar ejercicio físico regularmente. De hecho, la actividad física moderada aumenta la masa ósea y potencia la musculatura. Bailar, andar, correr, realizar ejercicios aeróbicos, subir escaleras o levantar pesos son algunas de las actividades a realizar por la población con riesgo de osteoporosis.
Tratamiento de los pacientes de edad avanzada con EII
Los criterios de los profesionales sanitarios para seleccionar el tratamiento y establecer las pautas a seguir por parte de los pacientes de edad avanzada con colitis ulcerosa o enfermedad de Crohn suelen ser similares a los tenidos en cuenta para determinar la medicación de cualquier otro grupo de la población. Incluso, la eficacia y los resultados que se pueden esperar de los fármacos también son análogos.
Sin embargo, cuando los pacientes mayores de 60 años presentan comorbilidades es posible que el impacto de los efectos adversos de los medicamentos sea mayor. En estos casos, los especialistas médicos cuentan en su arsenal terapéutico con opciones de tratamiento como la granulocito-monocito aféresis (GMA)5. Gracias a este tratamiento no farmacológico se eliminan de la sangre los leucocitos activados responsables de la inflamación intestinal de una manera muy segura para el paciente. De este modo se aumenta la seguridad y se reducen al máximo los riesgos en pacientes frágiles como las personas de edad avanzada.
- What is ulcerative colitis? – Adacyte
- https://educainflamatoria.com/pacientes-eii-edad-avanzada/
- Cinco claves para seguir una dieta adecuada si tengo colitis ulcerosa – Adacyte
- Relación entre la anemia y la Enfermedad Inflamatoria Intestinal – Adacyte
- Tratamiento de la colitis ulcerosa en pacientes dependientes de corticoides y fracaso previo a biológicos: Adacolumn® – Adacyte
Noticias
Cirugía en la colitis ulcerosa: antes, durante y después
8 de noviembre, 2022
Patient
Los médicos cuentan con un amplio arsenal terapéutico para tratar a los pacientes con colitis ulcerosa. Los fármacos disponibles mantienen la enfermedad inactiva o en remisión en la mayoría de casos. A pesar de ello, entre el 25 y el 40% de pacientes con colitis ulcerosa necesitará un tratamiento quirúrgico en algún momento de su enfermedad1.
A diferencia de la Enfermedad de Crohn2, la cirugía en la colitis ulcerosa es curativa. Y es que, al afectar al recto y al colon, su extirpación supone la curación total del paciente.
En concreto, la cirugía se indica3 uando el tratamiento farmacológico no ha controlado los síntomas de la colitis ulcerosa; si aparecen complicaciones como la estenosis (estrechamiento o reducción del diámetro interno del intestino), perforación, hemorragia grave, abscesos o fistulización; cuando se desarrollan lesiones premalignas o cancerígenas; o en caso de que exista enfermedad perianal y sea necesario realizar una cirugía de drenaje, colostomías derivativas para aislar las fístulas del paso de las heces o protectomías radicales en casos avanzados.
Preparación del paciente antes de la cirugía
El cirujano y el gastroenterólogo estudian el estado de evolución de la colitis ulcerosa en el paciente para conocer cuál es la extensión y la gravedad de los síntomas. A posteriori, le informan sobre la técnica más adecuada a su situación y sobre los beneficios, complicaciones y riesgos asociados a la misma4.
Antes de la cirugía5, se le realiza al paciente un estudio preoperatorio que consta de: análisis de sangre y orina, radiografía de tórax y electrocardiograma. Además, es muy importante que el paciente tenga un buen estado general y que suspenda el tratamiento que esté tomando (corticoides, inmunosupresores o terapia biológica, granulocitoaféresis…etc), si lo hubiera.
Dos días antes de la intervención, el paciente debe llevar una dieta líquida para que, con la ayuda de una preparación intestinal, se vacíe el intestino de desechos o restos de heces.
Intervenciones quirúrgicas en el tratamiento de la colitis ulcerosa
El gastroenterólogo y el cirujano pueden elegir entre diversas técnicas quirúrgicas para tratar la colitis ulcerosa6. Entre las más frecuentes destacan: la proctocolectomía total con ileostomía o con reservorio ileoanal. También es muy común realizar una colectomía total con anastomosis íleorectal, y la colectomía subtotal con ileostomía y fístula mucosa rectosigmoidea.
Cuando se realiza una proctocolectomía total, se resecciona todo el recto y el colon. Si se decide que sea una proctocolectomía total con ileostomía, se efectúa una abertura u orificio que comunique el íleon con el exterior (ileostomía) para eliminar los desechos intestinales en una bolsa (ostomía).
En el caso de que se los profesionales médicos se decanten por llevar a cabo una proctocolectomía restauradora o con reservorio ileoanal, se crea un reservorio o bolsa interna con parte del intestino delgado (íleon) que se unirá al ano y funcionará como un nuevo recto.
La técnica conocida como colectomía total con anastomosis íleorectal consiste en resecar todo el colon y unir (anastomosis) el íleon con el recto. Por su parte, en la colectomía subtotal con ileostomía y fístula mucosa rectosigmoidea se reseccionan solo las zonas afectadas del colon y se realiza una ileostomía. Si el sigma (parte final del colon) no está afectado, se deja intacto y se comunica con el exterior a través del ano o a través de una fístula mucosa realizada en la pared abdominal para que salgan las secreciones.
Qué ocurre después de la intervención quirúrgica en la colitis ulcerosa
Tras la cirugía en la colitis ulcerosa, llega la recuperación del paciente. En un principio no podrá ingerir ningún tipo de alimento. Sólo recibirá nutrientes a través de nutrición parenteral, por vía intravenosa. Una vez el tránsito intestinal se restablezca, podrá comenzar a ingerir gradualmente líquidos y, posteriormente, sólidos.
Asimismo, es habitual que el paciente evacúe restos de sangre, moco y/o heces a través del recto, en ocasiones, sin poder evitarlo. Es lo que se llama incontinencia rectal. Si el recto está intacto, no tendrá ningún dolor durante la evacuación. La frecuencia de estas secreciones irán disminuyendo con el paso del tiempo.
En el caso de tener una ostomía, el paciente debe empezar a acostumbrarse a su nueva situación cuanto antes. Su función intestinal estará alterada, cambiará su imagen corporal y tendrá un estoma. Durante su estancia hospitalaria, los profesionales sanitarios ayudarán al paciente y a su familia a adaptarse, ofreciéndoles todos los consejos e información que necesiten.
De todos modos, dados los cambios en al calidad de vida del paciente y las complicaciones que suelen asociarse después de esta cirugía, siempre se reserva como última alternativa y cuando el resto de tratamientos disponibles no han resultado efectivos en el control de la colitis ulcerosa.
- https://www.elsevier.es/es-revista-cirugia-espanola-36-articulo-estado-actual-del-tratamiento-quirurgico-S0009739X12003119
- Ulcerative colitis and Crohn similarities – Adacyte
- https://www.elsevier.es/es-revista-cirugia-espanola-36-articulo-estado-actual-del-tratamiento-quirurgico-S0009739X12003119
- https://www.educainflamatoria.com/que-preparacion-previa-tiene-una-cirugia-de-eii
- https://www.elsevier.es/es-revista-enfermedad-inflamatoria-intestinal-al-dia-220-articulo-manejo-perioperatorio-enfermedad-inflamatoria-intestinal-S1696780115000767
- What is ulcerative colitis? – Adacyte
Noticias
Tratamiento biológico de la Colitis Ulcerosa: una revolución terapéutica
13 de octubre, 2022
Patologías

Los últimos 30 años han supuesto una revolución en el tratamiento de la Enfermedad Inflamatoria Intestinal (EII). Los profesionales sanitarios han incorporado a su arsenal terapéutico nuevas moléculas que han demostrado una gran efectividad en
Enfermedad de Crohn y Colitis Ulcerosa. Además, estas moléculas han permitido ampliar las opciones terapéuticas con las que cuenta el paciente y avanzar hacia la Medicina Personalizada. Hablamos de los anticuerpos monoclonales.
Estos nuevos fármacos están basados en mecanismos de acción diferentes a los que estamos acostumbrados. Es por ello que permitirán, en un futuro muy cercano, manejar la enfermedad de una manera mucho más variada. Y es que, los expertos prevén que la mayor revolución en este campo está por llegar. Por el momento, están consiguiendo un tratamiento efectivo para los pacientes que sufren un brote moderado a grave y tienen una respuesta no favorable a tratamientos convencionales o con intolerancia y/o contraindicación a dichos tratamientos.
Qué son los tratamientos biológicos para la Colitis Ulcerosa
Los anticuerpos monoclonales son un tipo de proteína que se une a una citoquina (otro tipo de proteína) del organismo llamada Factor de Necrosis Tumoral alfa (TNF-alfa). De esta forma, el tratamiento biológico consigue bloquear la actividad del TNF. Y es que esta citoquina es una de las moléculas responsables del proceso inflamatorio cuando se produce un brote1 en pacientes con EII como la Colitis Ulcerosa.
Por lo tanto, nos referimos a compuestos complejos sintetizados a partir de un organismo o célula viva que se modifican genéticamente con tecnología e ingeniería genéticaes decir, por medio de biotecnología eficaz y precisa que permite la manipulación de esas células o microorganismos.
Así que se puede afirmar que el tratamiento biológico de la Colitis Ulcerosa mejora la calidad de vida de los pacientes. Es decir, a diferencia de los demás medicamentos existentes, estos nuevos fármacos biológicos permiten mantener la enfermedad en remisión durante períodos más prolongados. De esta forma, el paciente puede llevar a cabo sus actividades cotidianas de manera normal sin presentar ningún tipo de síntoma.
Cuándo y cómo se administra un fármaco biológico
Los fármacos biológicos están indicados tanto para la inducción como para la remisión de la Colitis Ulcerosa. Antes de recomendar su administración, el profesional sanitario se centrará en conocer el estado de vacunación del paciente y el de inmunización frente a algunas infecciones. Además, descartará una infección latente por tuberculosis. Si el paciente estuviera en esta situación, las bacterias responsables de la tuberculosis estarían vivas en su organismo pero inactivas. Por lo tanto, no tendría síntomas hasta que el virus se activara. Para descartar esta posibilidad se realizan pruebas como una radiografía de tórax, un análisis de sangre y la prueba de la tuberculina (mantoux).
Posteriormente, el médico evaluará qué fármaco biológico administrar al paciente de todo el arsenal disponible. Seguidamente, se establecerá la dosis y se valorará cuál es el momento más adecuado para iniciar el tratamiento biológico de la Colitis Ulcerosa con fármacos biológicos.
- Intravenosa. El fármaco se administra en el hospital a través de una vía venosa. La administración será lenta para evitar una reacción al medicamento. Se administran así infliximab, su biológico y vedolizumab.
- Subcutánea. El fármaco se lo puede administrar el propio paciente en casa como si se tratara de una inyección de insulina. Adalimumab y golimumab se administran con este método.
En el caso de ustekinumab, la primera dosis se administra mediante la vía intravenosa. Las dosis posteriores se aplican mediante vía subcutánea.
Diversidad de tratamientos biológicos para la Colitis Ulcerosa
La aprobación de infliximab marcó un punto de inflexión en el tratamiento de los pacientes con Enfermedad Inflamatoria Intestinal en general y para la Colitis Ulcerosa en particular. Y es que suponía la llegada a manos del médico de la primera formulación de esta familia de medicamentos. Pero no ha sido el único tratamiento biológico aprobado.
Existen otros principios activos pertenecientes al grupo de los anticuerpos anti-factor de Necrosis Tumoral o fármacos anti-TNF. Es el caso de adalimumab y de golimumab, así como de los biosimilares de infliximab y de adalimumab.
Por su parte, vedolizumab es un fármaco antagonista de receptores de integrina. El objetivo de este principio activo es disminuir la entrada de células inflamatorias al intestino. Y lo hace bloqueando las integrinas, receptores de membrana que permiten el paso de glóbulos blancos y linfocitos al intestino.
Uno de los últimos fármacos biológicos aprobados ha sido ustekinumab. En este caso, se centra en el bloqueo de la acción de las interleucinas 12 y 23. Son proteínas reguladoras de la respuesta inflamatoria. Cuando están elevadas se produce una activación y una proliferación linfocitaria provocando, a su vez, una respuesta inflamatoria del organismo.
Efectos secundarios del tratamiento biológico en Colitis Ulcerosa
Normalmente los efectos secundarios de los fármacos biológicos son leves. Es habitual que los pacientes puedan sentir cansancio, algunas reacciones cutáneas, náuseas, vómitos, dolor en las articulaciones o en los músculos y fiebre3.
Cuando el tratamiento biológico se realiza mediante administración intravenosa con infliximab, adalimumab o golimumab, el paciente puede referir alguna reacción. Por ejemplo, dificultad para respirar, urticaria, enrojecimiento, picor e hinchazón en labios y garganta o dolor de cabeza. Si esto ocurriera, se pararía la infusión para reanudarla con una velocidad menor. En las siguientes administraciones, se premedicaría al paciente con corticoides.
Por su parte, los pacientes tratados con adalimumab o golimumab pueden tener reacción cutánea en la zona de la inyección subcutánea En general, todos los fármacos biológicos pueden incrementar las posibilidades de sufrir infecciones, sobre todo respiratorias. Por ello, los profesionales sanitarios recomiendan llevar al día todas las vacunas. Y, en caso de tener algún síntoma de inicio de la infección como fiebre o tos, es recomendable informar de ello al médico.
Noticias
DÍA MUNDIAL DE LA SEGURIDAD DEL PACIENTE
16 de septiembre, 2022
Patient

El Día Mundial de la Seguridad del Paciente, se establece por primera vez en el año 2019 de la mano de la Asamblea Mundial de la Salud1. Esta celebración pretende despertar una mayor concienciación y participación de la sociedad, ampliar los conocimientos en todo el mundo y fomentar la solidaridad y la adopción de medidas para promover la seguridad del paciente a nivel mundial.
En línea con este planteamiento, cada año se destaca un tema concreto sobre el cual hacer hincapié para reducir daños evitables que se pudieran causar a pacientes y en búsqueda de una cobertura sanitaria internacional. Además, se ha elaborado el “Global Patient Safety Action Plan 2021-2030”2 con la misión Impulsar políticas, estrategias y acciones, basadas en la ciencia, experiencia del paciente, y asociaciones, para eliminar las fuentes de riesgo y daño evitables para los pacientes y los trabajadores de la salud.
Objetivos pasados del Día Mundial de la Seguridad del Paciente
- 2019: concienciar sobre la importancia de la seguridad de los pacientes e instar a los ciudadanos a demostrar su compromiso con esta causa bajo el lema “Alcemos la voz por la seguridad del paciente”3.
- 2020: de nuevo afectados por el contexto de pandémico a causa de la COVID-19, la campaña se centra en el tema de la seguridad del personal sanitario como pilar básico para poder asegurar la seguridad de los pacientes; y así lo determinaba “Seguridad del personal sanitario: Una prioridad para la seguridad de los pacientes«4.
- 2021: se hace hincapié en la carga significativa de perjuicios causados a las mujeres y los recién nacidos a los que se presta una atención materno-infantil no exenta de riesgos, sobre todo en el momento del parto, que es cuando se ocasionan la mayor parte de los daños. Esta cuestión es especialmente importante habida cuenta de la perturbación de los servicios de salud causada por la pandemia de COVID-19, que ha agravado este problema. «Atención Materna y Neonatal Segura»5.
Objetivos del Día Mundial de la Seguridad del Paciente de 2022
Para el 2022, el tema de la campaña es la seguridad de la medicación bajo el lema “Medicación sin daño”, teniendo en cuenta que todas las personas en su vida tomarán medicación para tratar o prevenir un problema de salud. Sin embargo, a veces los medicamentos pueden causar graves daños si no se almacenan bien, si se prescriben o toman de manera incorrecta o si no se controlan de forma suficiente.
Así, a continuación detallamos los objetivos6 que conforman la campaña de este año establecidos por la OMS (Organización Mundial de la Salud):
- AUMENTAR la concienciación mundial sobre la elevada carga de daños relacionados con los medicamentos debido a errores de medicación y prácticas inseguras, y ABOGAR por la adopción de medidas urgentes encaminadas a mejorar la seguridad de la medicación.
- IMPLICAR a las principales partes interesadas y a los asociados en los esfuerzos para prevenir los errores de medicación y reducir los daños relacionados.
- EMPODERAR a pacientes y familiares para que participen activamente en el uso seguro de los medicamentos.
- AMPLIAR la aplicación del Reto Mundial por la Seguridad del Paciente: Medicación sin daño.
Video de la campaña del Día Mundial de la Seguridad del Paciente: 17 de septiembre 2022.
- https://www.who.int/es/about/governance/world-health-assembly
- https://www.who.int/publications/i/item/9789240032705
- https://www.who.int/es/campaigns/world-patient-safety-day/2019
- https://www.who.int/es/campaigns/world-patient-safety-day/2020
- https://www.who.int/es/campaigns/world-patient-safety-day/2021
- https://cdn.who.int/media/docs/default-source/campaigns-and-initiatives/patient-safety/announcing-world-patient-safety-day-2022-es.pdf?sfvrsn=c5e32a09_34
ContáctanosPara solicitar información adicional
Contáctanos